
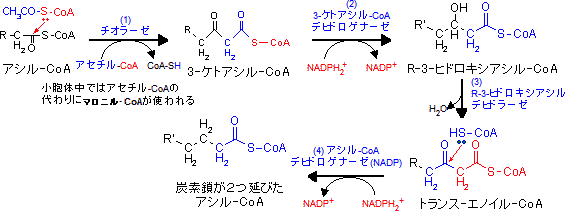
脂肪酸合成の個々の反応を見れば脂肪酸の酸化的異化代謝(b-酸化)に出てくる反応と類似しているが,経路は逆反応と同じではない(「異化と同化は別経路」の例)。以下に,両者の異なる点を示す。
- 脂肪酸のb-酸化と異なり,脂肪酸の生合成は細胞質で行われる。
- 脂肪酸分解の逆反応としてアセチル-CoAを直接利用するのではなく,一旦,マロニル-CoAがつくられ,CO2を放出してアセチル基が脂肪酸の鎖に転移する。CO2はマロニル-CoAの合成に再利用される。
この理由として,b-酸化の
3-オキソアシル-CoA + CoA  アシル-CoA + アセチル-CoA
アシル-CoA + アセチル-CoA
の平衡が大きく右に偏っているため,アセチル-CoAでは自由エネルギー的に不利で,合成には用いられない。
- b-酸化の補酵素(FAD,NAD+)と異なり,生合成ではペントースリン酸経路から供給されるNADP+が利用される。
- β-酸化の場合のCoAの代わりに,脂肪酸は4'-ホスホパンテテインを補因子として結合したアシルキャリアプロテイン(ACP)*のSH基にチオエステル結合する。動物の酵素の場合,ACPは脂肪酸合成酵素(脂肪酸シンターゼ)の一部である。
* 大腸菌の酵素は脂肪酸合成酵素複合体を形成している。アシルキャリアプロテイン(ACP)は分子量10,000の小型タンパク質。
- b-酸化の場合のS(L)-3-ヒドロキシアシル-CoAに相当するものは,生合成ではR(D)-3-ヒドロキシアシル-ACPである。
動物の場合,脂肪酸合成はパルミトイル(C16)-ACPまでで終わる。パルミトイル-ACPはパルミトイル-ACPヒドラターゼ(動物ではチオエステラーゼドメイン)によって加水分解されてACP部分が切り離され,パルミチン酸が生成する。
脂肪酸の生合成はクエン酸により促進される。クエン酸がTCA回路に使われるか,ミトコンドリア膜を出て脂肪酸の生合成に使われるかは,イソクエン酸デヒドロゲナーゼの活性(ADPによって活性化され,ATPによって阻害される)により調節される。この酵素活性が抑制されるとTCA回路がslow
downし,クエン酸が蓄積する(→ アセチル-CoA カルボキシラーゼの活性化, 下記)。
また,ミトコンドリアを出たクエン酸は次の経路によって脂肪酸合成に必要なNADPH2+の約40%を供給する(残りの60%はホスホグルコン酸回路, HMSから供給される)。

アセチル-CoA カルボキシラーゼは脂肪酸合成の最初の反応
(1)を触媒し,また,この段階が合成の律速段階の1つである。哺乳類と鳥類の酵素は単量体では不活性であるが,分子量4〜8百万の繊維状ポリマーを形成し活性型になる。
単量体(プロトマー,不活性)

重合体(ポリマー,活性)
長鎖アシル-CoAはこの平衡を左にずらし(フィードバック阻害),クエン酸は右にずらす。原核生物では脂肪酸はすぐにリン脂質の合成に使われるため,脂肪酸の蓄積が起こらず,アセチル-CoA
カルボキシラーゼはこのような制御を受けない。
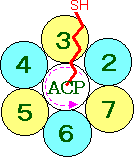
 反応(2)〜(7)を触媒する脂肪酸シンターゼ(fatty acid synthase)は,大腸菌や葉緑体では7つの酵素が必要である。これらの酵素は複合酵素系(multi enzyme system)を形成し,合成の効率を上げている。
反応(2)〜(7)を触媒する脂肪酸シンターゼ(fatty acid synthase)は,大腸菌や葉緑体では7つの酵素が必要である。これらの酵素は複合酵素系(multi enzyme system)を形成し,合成の効率を上げている。
 |
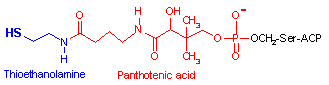
ACPの4'-ホスホパンテテイン補因子
赤で示した部分は補酵素Aの一部と同じである。 |
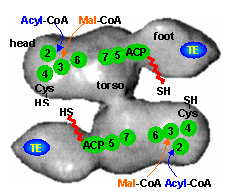
 哺乳動物のの酵素は巨大なタンパク質で,全ての触媒作用は同一のタンパク質上の異なる領域で遂行されるという多機能酵素(multifunctional enzyme)の一種である。ヒトの脂肪酸シンターゼの立体構造が電子顕微鏡で観察され,3つの領域から成ることが示された。これが2つ,頭(head)と足(foot)で向き合い,胴体(torso)で結合した分子量544,000のホモ二量体型タンパク質である。各サブユニットの胴体ドメインのSer残基に4'-ホスホパンテテインが共有結合しており,これがACPの実体である。4'-ホスホパンテテインのSH基に結合した脂肪酸はの活性部位ドメイン(2)〜(7)を順次巡ることによって,脂肪酸の鎖長が伸びていきパルミチン酸がつくられる。分子の構造から見て,2分子の脂肪酸が同時につくられていく。最終的に,パルミチン酸はfoot領域のチオエステラーゼ(TE)で切り取られて遊離する。
哺乳動物のの酵素は巨大なタンパク質で,全ての触媒作用は同一のタンパク質上の異なる領域で遂行されるという多機能酵素(multifunctional enzyme)の一種である。ヒトの脂肪酸シンターゼの立体構造が電子顕微鏡で観察され,3つの領域から成ることが示された。これが2つ,頭(head)と足(foot)で向き合い,胴体(torso)で結合した分子量544,000のホモ二量体型タンパク質である。各サブユニットの胴体ドメインのSer残基に4'-ホスホパンテテインが共有結合しており,これがACPの実体である。4'-ホスホパンテテインのSH基に結合した脂肪酸はの活性部位ドメイン(2)〜(7)を順次巡ることによって,脂肪酸の鎖長が伸びていきパルミチン酸がつくられる。分子の構造から見て,2分子の脂肪酸が同時につくられていく。最終的に,パルミチン酸はfoot領域のチオエステラーゼ(TE)で切り取られて遊離する。
 |
| [哺乳類の脂肪酸合成酵素のドメイン構造] |
 |
 |
| [脂肪酸合成酵素二量体の立体図] |
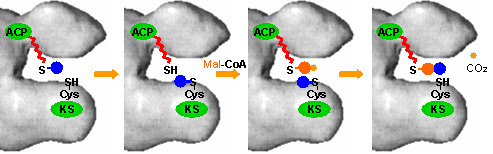
[反応(2)〜(4)の機構] 青と橙の丸はアシル基 |
- 細胞質でつくられた脂肪酸は,さらにミトコンドリアや小胞体で炭素数を増すことができる。
- パルミチン酸(C16)
 C18
C18 C20
C20 C22
C22 C24
C24
- これは,β-酸化の逆反応を利用してなされる。ただし,エノイル-CoAの還元段階(4)はβ-酸化の場合のFADH2ではなくて NADPH2+を利用し,アシル-CoAデヒドロゲナーゼ(NADP)が触媒する。
動物の肝滑面小胞体において,NADH2およびO2の存在下,パルミトイル-CoAとステアロイル-CoAは不飽和化される。高等動物は二重結合を2つ以上もつ脂肪酸を合成できない。従って,リノール酸やリノレン酸は食物から補給する必要がある(ビタミンF)。リノール酸はアラキドン酸の重要な原料である。
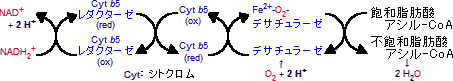







 アシル-CoA + アセチル-CoA
アシル-CoA + アセチル-CoA





重合体(ポリマー,活性)



 反応(2)〜(7)を触媒する脂肪酸シンターゼ(fatty acid synthase)は,大腸菌や葉緑体では7つの酵素が必要である。これらの酵素は複合酵素系(multi enzyme system)を形成し,合成の効率を上げている。
反応(2)〜(7)を触媒する脂肪酸シンターゼ(fatty acid synthase)は,大腸菌や葉緑体では7つの酵素が必要である。これらの酵素は複合酵素系(multi enzyme system)を形成し,合成の効率を上げている。 哺乳動物のの酵素は巨大なタンパク質で,全ての触媒作用は同一のタンパク質上の異なる領域で遂行されるという多機能酵素(multifunctional enzyme)の一種である。ヒトの脂肪酸シンターゼの立体構造が電子顕微鏡で観察され,3つの領域から成ることが示された。これが2つ,頭(head)と足(foot)で向き合い,胴体(torso)で結合した分子量544,000のホモ二量体型タンパク質である。各サブユニットの胴体ドメインのSer残基に4'-ホスホパンテテインが共有結合しており,これがACPの実体である。4'-ホスホパンテテインのSH基に結合した脂肪酸はの活性部位ドメイン(2)〜(7)を順次巡ることによって,脂肪酸の鎖長が伸びていきパルミチン酸がつくられる。分子の構造から見て,2分子の脂肪酸が同時につくられていく。最終的に,パルミチン酸はfoot領域のチオエステラーゼ(TE)で切り取られて遊離する。
哺乳動物のの酵素は巨大なタンパク質で,全ての触媒作用は同一のタンパク質上の異なる領域で遂行されるという多機能酵素(multifunctional enzyme)の一種である。ヒトの脂肪酸シンターゼの立体構造が電子顕微鏡で観察され,3つの領域から成ることが示された。これが2つ,頭(head)と足(foot)で向き合い,胴体(torso)で結合した分子量544,000のホモ二量体型タンパク質である。各サブユニットの胴体ドメインのSer残基に4'-ホスホパンテテインが共有結合しており,これがACPの実体である。4'-ホスホパンテテインのSH基に結合した脂肪酸はの活性部位ドメイン(2)〜(7)を順次巡ることによって,脂肪酸の鎖長が伸びていきパルミチン酸がつくられる。分子の構造から見て,2分子の脂肪酸が同時につくられていく。最終的に,パルミチン酸はfoot領域のチオエステラーゼ(TE)で切り取られて遊離する。

 C18
C18 C20
C20 C22
C22 C24
C24