

|
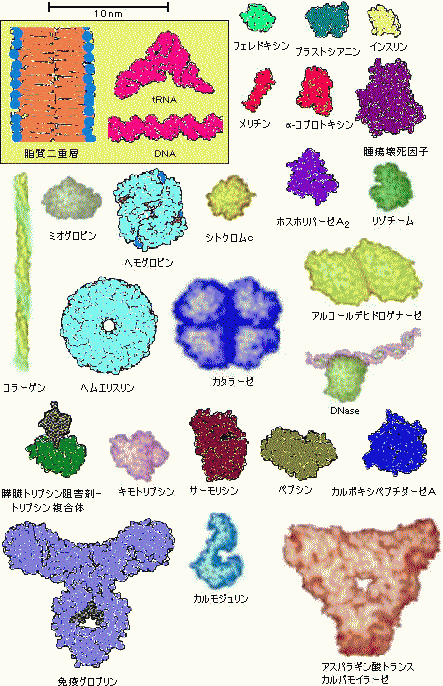
アミノ酸 ペプチド タンパク質 タンパク質の機能と変性 天然変性タンパク質 |

|
|
|
 |
  |
|
|
|
 |
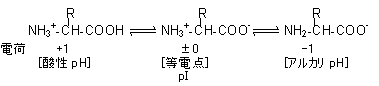 |
|
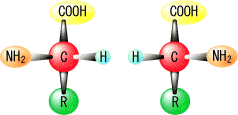
| 天然のアミノ酸はL型 | D-アミノ酸 | アミノ酸の等電点(isoelectric point, pI) |
| アミノ酸の立体化学 グリシンにはL,Dの区別はない。 | ||
 |
|
| アミノ酸 | 酸 |
pKa |
| a-カルボキシル基 | 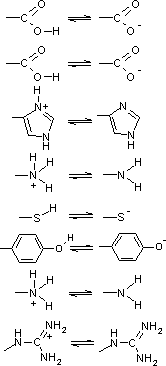 |
3.1 |
| Asp, Glu | 4.1 | |
| His | 6.0 | |
| a-アミノ基 | 8.0 | |
| Cys | 8.3 | |
| Tyr | 10.9 | |
| Lys | 10.8 | |
| Arg | 12.5 |
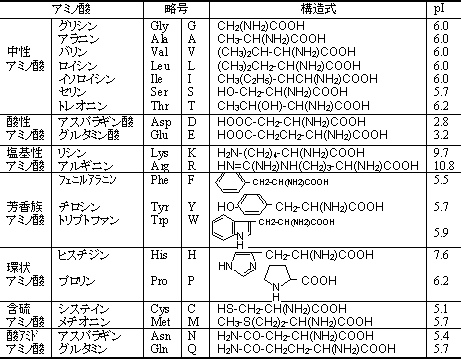
 個々のアミノ酸残基の特徴
個々のアミノ酸残基の特徴
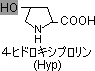
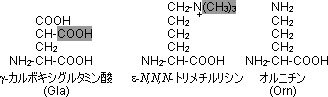
|
|
|
 |
  |
|
|
|
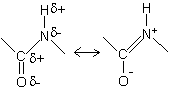
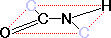
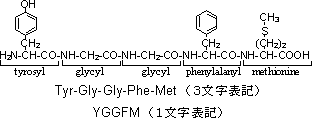
| 種類 | 例 |
| 1) ホルモンペプチド | インシュリン,オキシトシン, アンジオテンシンⅡ |
| 2) 抗生物質 (D-アミノ酸や特殊アミノ酸を含むものが多い) |
ペニシリン,グラミシジンS |
| 3) 酵素阻害ペプチド | ロイペプチン,ペプスタチン, 植物トリプシンインヒビター |
| 4) 神経伝達物質 | メチオニンエンケファリン, サブスタンス P |
| 5) 呈味ペプチド | アスパルテーム |
| 6) 毒ペプチド | AM-トキシン,アマニチン, コブラトキシン |
| 7) その他 | グルタチオン(細胞内還元剤) |
|
|
|
 |
  |
|
|
|
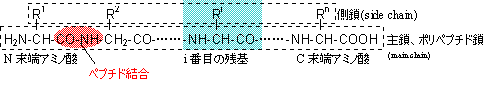
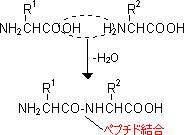
 1次構造(primary structure)
1次構造(primary structure)
|
| タンパク質 | 等電点 |
| 血清α1-グロブリン ハプトグロブリン 血清アルブミン 血清γ1-Globulin フィブリノーゲン ヘモグロビン 血清γ2-グロブリン ペプシン 卵白アルブミン インシュリン ヒストン リボヌクレアーゼ シトクロームc リゾチーム |
2.0 4.1 4.7 5.8 5.8 7.2 7.4 1.0 4.6 5.4 7.5-11.0 9.6 9.8 11.1 |
 2次構造(secondary structure)
2次構造(secondary structure) 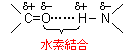
 なぜタンパク質は2次構造をとるのか?
なぜタンパク質は2次構造をとるのか?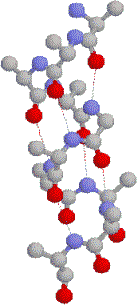 |
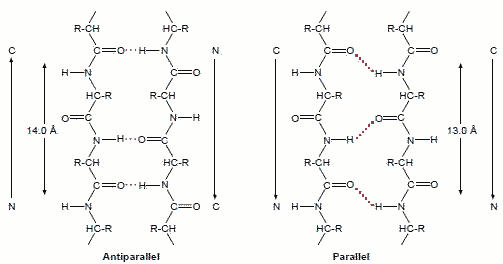 |
| a-helix | b-sheet |
 a-helixの特徴
a-helixの特徴 b-sheetの特徴
b-sheetの特徴
 3次構造(tertiary structure)
3次構造(tertiary structure) 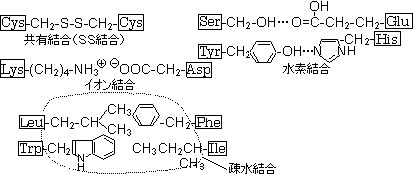
 |
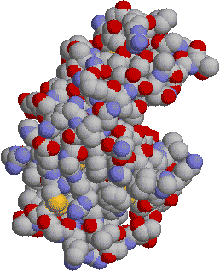 |
| 卵白リゾチームの3次構造。 左は主鎖だけをリボンで表したもの。赤,a-helix,橙,b-sheet 右は全ての原子を空間充填モデルで表したもの。 |
|
 4次構造(quarternary structure)
4次構造(quarternary structure)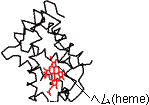 ヘモグロビンの1つの サブユニットの3次構造 |
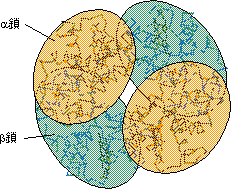 ヘモグロビンの4次構造 |
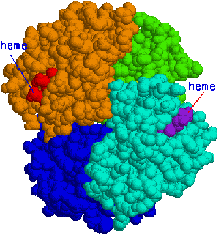 |
 ドメイン(domain)の概念
ドメイン(domain)の概念 いくつかのドメインの例: いくつかのドメインの例: |
||
 |
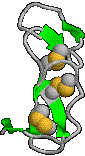 |
 |
| 免疫グロブリンドメイン 7本のb-sheetが樽状に配置 |
EGFドメイン 3つのS-S結合が 上下に並んでいる |
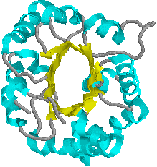
a/bバレルドメイン |
| 橙色は,シスチン残基の硫黄原子 | ||
 |
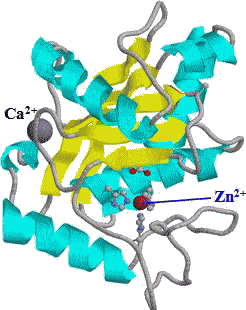 |
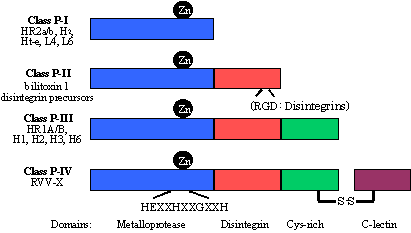
| 蛇毒メタロプロテアーゼは複数のドメインから成る | メタロプロテアーゼドメインの構造 |
| それぞれのドメインを色を変えて示す。 青,メタロプロテアーゼドメイン; 赤,ディスインテグリンドメイン; 緑,Cyrichドメイン; 紫,C型レクチンドメイン |
 タンパク質の1次構造の決定
タンパク質の1次構造の決定| 構造未知のタンパク質 ↓精製 純粋なタンパク質 ↓還元剤でSS結合を切り、化学修飾する ↓いくつかのタンパク分解酵素で分解する 多くのペプチド断片 ↓分離・精製する ↓各断片のアミノ酸配列を決める ↓各断片の並び方を推定する タンパク質の全1次構造 |
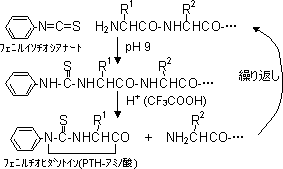 |
| エドマン分解 |
|
|
|
 |
  |
|
|
|
| 分類 | 機能 | 例 |
| 1) 酵素 2) 酵素阻害剤 3) 情報タンパク質 4) ホルモン 5) 輸送タンパク質 6) 防御タンパク質 7) 運動タンパク質 8) 毒タンパク質 9) 貯蔵タンパク質 10)構造タンパク質 |
触媒作用 酵素作用を阻害 細胞内情報伝達 細胞間情報伝達 物質輸送 生体防御 細胞の運動性 細胞毒 貯蔵栄養 細胞や細胞間の構築 |
トリプシン、乳酸脱水素酵素 マクログロブリン、トリプシンインヒビター ホルモン受容体 インシュリン、成長ホルモン ヘモグロビン、リポタンパク質 免役グロブリン、フィブリノーゲン アクチン、ミオシン 蛇毒タンパク質、リシン グリシニン、カゼイン コラーゲン、膜タンパク質、ウィルス殻タンパク質 |
| 非アミノ酸成分 | 例 | |
| 核タンパク質 | 核酸 | ヒストン、プロタミン |
| リポタンパク質 | 脂質 | 血清リポタンパク質 |
| 糖タンパク質 | 糖質 | グリコホリン、免役グロブリン |
| 色素タンパク質 | 色素(ヘムなど) | シトクローム、ヘモグロビン |
| 金属タンパク質 | 金属イオン | トランスフェリン、フェリチン,メタロプロテアーゼ |
 |
弱く加熱 冷却 |
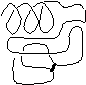 |
強く加熱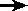 |
 |
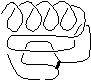
| 生の(native)タンパク質 [活性100%] |
部分変性状態 [低活性] |
完全変性状態 [不活性] |
||
| [タンパク質の変性] | ||||

|

|